Complications thrombotiques des techniques d’oblitération saphène endovasculaire

Complications thrombotiques des techniques d’oblitération saphène endovasculaire
RÉSUMÉ
Aujourd’hui l’efficacité des techniques endovasculaires : radiofréquence ou laser endoveineux (LEV) n’est plus discutable. La morbidité, grâce à de meilleures indications et de meilleures pratiques, est très faible ; il reste pourtant un faible risque d’extension thrombotique (ET) fémorale ou poplitée. Concernant le cathéter ClosurePlus® la première étude de 223 cas a rapporté 3 complications thrombo-emboliques. Ces mêmes patients se retrouvent dans les nombreuses études successives appelées « Groupe Closure® ». A côté de celle-ci d’autres études ne rapportent pas d’ET. Seules quelques études ont rapporté des ET plus souvent dans le cas de patients âgés ou dans des groupes élevés de classe CEAP. Aujourd’hui aucune ET n’a été rapportée pour le cathéter ClosureFASTTM. Concernant le LEV, très peu d’études ont rapporté des ET ; c’est plus souvent dans le traitement de la petite veine saphène, dans le cas de patients âgés ou dans des groupes élevés de classe CEAP. Pour le LEV le risque est d’environ 1 %, pour la ClosurePlus® le risque presque nul et pour le cathéter ClosureFASTTM il devrait se situer plus près du LEV que du cathéter ClosurePlus®. Ce risque diminue avec la courbe d’apprentissage.
SUMMARY
At present the efficacy of endovascular technique: Radiofrequency (RF) and endovenous laser (EVL) is unquestionable. The short term morbidity remains the possible risk of thrombus extension (TE) in the common femoral or popliteal vein. Concerning ClosurePlus® a first study of 223 patients included in the « Closure® group » reported 3 TE. These same patients were reported in many studies until the last revue of a register of 1222 patients. In addition many other series reported no TE. Only very few studies reported TE usually in case of old patients, with CEAP class up to 4. At present no TE were reported with ClosureFASTTM. About EVL the majority of published series did not report any TE. Only very few studies have reported TE usually concerning old patients, short saphenous vein, high CEAP class. For EVL the percentage is around 1 %, lower for ClosurePlus® and still non evaluated for ClosureFASTTM. This risk is decreasing with the learning curve.
INTRODUCTION
La chirurgie endoluminale des varices fait partie des procédures nouvelles qui permettent d’obtenir la destruction du tronc saphène sans en réaliser l’ablation chirurgicale [1]. Il existe deux techniques qui utilisent la chaleur pour détruire l’endothélium et le collagène de la paroi veineuse, les procédures qui utilisent les propriétés de la radiofréquence et celles qui utilisent le laser. Toutes les deux, par l’énergie thermique qu’elles fournissent, permettent d’obtenir une rétraction fibreuse de la veine et son occlusion. Leur efficacité respective aujourd’hui n’est plus discutable : elles permettent d’obtenir entre 90 et 100 % d’oblitération qui reste stable avec les années.
Après la courbe d’apprentissage et une meilleure expérience de ces techniques, la morbidité précoce est devenue très faible, les brûlures de l’une ou l’autre des techniques, ainsi que les paresthésies induites par la radiofréquence, ont disparu du fait d’une bonne connaissance des indications. Il reste actuellement la douleur postopératoire qui obère parfois de façon importante la qualité de vie postopératoire de la procédure laser, et concernant les deux techniques, un très faible risque d’extension thrombotique veineuse profonde (ETVP) qui fera l’objet de cette revue de la littérature.
Nous disposons actuellement de nombreuses études à court terme. L’analyse de ces complications est globalement plus facile pour la radiofréquence en raison du matériel et d’une procédure plus standardisée.
Globalement, parmi ces complications postopératoires thrombo-emboliques, il faut différencier les complications simplement dues à la chirurgie, c’est-à-dire les thromboses veineuses profondes (TVP) fémorales, poplitées ou musculaires, jumelles ou soléaires et les complications proprement dues à la technique endovasculaire c’est-à-dire les ETVP concernant surtout la jonction saphéno-fémorale (JSF) avec extension du thrombus au niveau de la veine fémorale commune (VFC).
PRINCIPE ET MODE D’ACTION DES DIFFÉRENTES PROCÉDURES
Il est important de bien comprendre le fonctionnement de chaque technique afin d’évaluer les risques d’extension du traumatisme opératoire et de la thrombose vers la VFC.
Radiofréquence
Le principe de la radiofréquence consiste à utiliser la résistance naturelle de la paroi veineuse pour provoquer, lors du passage d’un courant de très hautes fréquences dans cette paroi veineuse, entre deux pôles + et –, une élévation thermique contrôlée. Cette énergie thermique contrôlée qui élève la température au niveau de la paroi vasculaire est induite de façon très précise par le passage de ce courant entre deux pôles électriques.
Compte tenu de la forme des deux cathéters, ClosurePlus® 8 F et 6 F, l’élévation thermique s’effectue sur la hauteur d’un disque circulaire de 3 mm de hauteur. Cette diffusion de température est fonction de la distance qui sépare les électrodes (Photo 1). L’échauffement de la paroi vasculaire à 85° produit la destruction de l’intima sur toute sa surface ainsi qu’un épaississement et une contraction des fibres collagènes présentes dans la média et l’adventice. Le point de départ d’échauffement du cathéter ClosurePlus® est donc extrêmement précis.
Ce phénomène de contraction aboutit secondairement à l’évolution fibreuse et à l’occlusion de la lumière veineuse. La procédure étant réalisée sur une veine vide de sang, la formation de thrombus à ce niveau est réduite au minimum.
Le cathéter ClosureFASTTM utilise les mêmes propriétés de la radiofréquence pour chauffer la veine mais sur une longueur de 7 cm à 120° (Photo 2) ; la partie chauffante du cathéter est recouverte d’une substance non adhésive (téflon®) qui l’empêche d’adhérer sur la paroi veineuse lors du chauffage. Lorsque l’extrémité du cathéter est correctement positionnée, l’énergie radiofréquence est délivrée pendant 20 secondes, deux fois de suite, puis le cathéter estretiré de 6,5 cm pour continuer le traitement segmentaire du tronc saphène.
Laser endoveineux
Le matériel, actuellement commercialisé par plusieurs firmes, propose des lasers allant de 810 nm jusqu’à 2068 nm ; les plus utilisés étant les lasers 810 nm, 940 nm et 980 nm.
Concernant cette technique, il n’y a malheureusement pas de consensus précis quant à la puissance à utiliser, le nombre de tirs, la durée de chaque tir, l’intervalle entre chaque tir en fonction du diamètre de la veine à traiter. Ceci rend particulièrement difficile l’analyse des résultats. Il n’y a pas non plus de consensus concernant la nécessité ou non de procéder sur une veine exsangue ou contenant du sang. Certains auteurs ont, en effet, montré que, du fait de la courbe d’absorption des longueurs d’onde utilisées, l’énergie permettait d’obtenir par l’ébullition du sang une brûlure pariétale par contact [2].
D’autres études [3] ont montré, au contraire, que l’efficacité était meilleure lorsque le tronc veineux était exsangue. L’échauffement se produit plus au niveau d’une sphère lumineuse de chaleur située à l’extrémité de la fibre que sur le prolongement d’un rayon lumineux sortant à l’extrémité de la fibre (Photo 3). Quoi qu’il en soit, il semble que l’échauffement produit à l’extrémité de la fibre soit moins précis en surface que celui produit par le cathéter ClosurePlus®. Lors de la procédure, la veine traitée n’étant pas exsanguinée, la conversion de la lumière laser en chaleur se fait par diffusion optique ; l’énergie laser délivrée dans le sang provoque des bulles de vapeur générées par le sang hémolysé. Ce sont les bulles qui transmettent l’énergie thermique à la totalité de la circonférence de la paroi interne veineuse. La température moyenne mesurée à l’extrémité de la fibre laser est de 729 °C [4]. La limite de diffusion de chaleur et donc moins précise qu’avec la radiofréquence utilisant ClosurePlus®.
INTRODUCTION ET POSITIONNEMENT
Ces trois techniques nécessitent d’introduire un cathéter au niveau du tronc de la grande saphène, habituellement sous le genou, soit par une mini-incision de phlébectomie, soit par ponction directe échoguidée. Il est parfois nécessaire de monter un guide hydrophile en J (guide-wire) dont la position est contrôlée par écho-Doppler. Un introducteur est ensuite mis en place sur le guide, il servira à monter le cathéter 5 F qui permettra le passage de la fibre laser ou du cathéter ClosurePlus® ou ClosureFASTTM. Le repérage de l’extrémité du cathéter ou de la fibre est un élément essentiel de la procédure. Il s’effectue habituellement par écho-Doppler per-opératoire à l’aide de gel et d’une housse stérile. Le repérage se fait à l’aide d’une sonde superficielle 7,5-12 MHz en repérage transversal et longitudinal.
Le cathéter ClosurePlus® est habituellement assez facilement visible en coupe longitudinale. Introduit dans la VFC, les électrodes sont déployées et le retrait progressif du cathéter permet de positionner les électrodes juste en-dessous de la veine épigastrique.
Concernant le cathéter ClosureFASTTM, son repérage est en général un peu plus difficile car, si le plan d’exploration n’est pas rigoureusement parallèle à celui du cathéter, on peut tout à fait prendre la coupe distale du cathéter pour son extrémité (son extrémité pouvant être beaucoup plus proximale). Il est donc important de faire avancer et reculer le cathéter pour parfaitement voir son extrémité ; elle doit être positionnée en-dessous de la veine épigastrique, en général 2 cm avant la valve terminale.
Concernant la fibre laser, bien que son extrémité soit en général un point plus brillant en exploration longitudinale, il faut aussi toujours se méfier d’un plan de coupe oblique qui donnerait l’illusion de l’extrémité de la fibre. Après recul de la fibre, elle doit être positionnée 2 cm avant la valve terminale.
FRÉQUENCE DES COMPLICATIONS THROMBO-EMBOLIQUES
D’un point de vue général, l’étude des séries ayant rapporté des complications thrombo-emboliques doit tenir compte des différents facteurs de risques habituels de la chirurgie veineuse, à savoir : le mode d’anesthésie (anesthésie générale ou anesthésie locale), la durée de séjour en milieu hospitalier ou ambulatoire, les éventuels antécédents de troubles de la coagulation, les éventuels traitements HBPM postopératoires. A cela s’ajoute le fait que seules les thromboses vérifiées, situées au niveau de la jonction saphéno-fémorale peuvent être en rapport avec la technique endovasculaire. En effet, il est parfois fait état de complications thrombo-emboliques qui concernent les veines jumelles ou la veine poplitée.
Radiofréquence
Concernant l’étude des procédures utilisant la radiofréquence, toutes concernent le cathéter ClosurePlus®. Les nombreuses séries ayant rapporté les complications thrombo-emboliques sont des séries qui concernent le même groupe de patients. Il s’agit d’un groupe de patients inclus dans différents centres en Europe et aux Etats-Unis depuis la fin des années 98 et qui ont été étudiés régulièrement au fur et à mesure de l’inclusion de nouveaux patients. Tous les patients inclus dans ce registre devaient avoir un examen échoDoppler de la JSF dans la première semaine postopératoire. Cette étude appelée « Groupe Closure® » a été revue pour la première fois par Chandler [5] ; elle concerne les 223 premiers patients : elle a rapporté 3 ETVP au niveau de la VFC dont une embolie pulmonaire. Ces 3 ETVP asymptomatiques avaient été dépistées quelques jours après la procédure ; un patient était porteur d’une entorse et était resté alité plusieurs jours, ce patient a fait une embolie pulmonaire à J7 ; une de ces procédures avait été faite avec un simple repérage manuel sans repérage écho-Doppler. Toutes ont été traitées efficacement par HBPM. Il est remarquable de noter que ces trois ETVP sont survenues sur les 94 premiers patients inclus dans ce groupe. Plus tard, ce même groupe de patients avec des nouvelles inclusions a été étudié par d’autres auteurs : Chandler [6], Merchant [7-9], Manfrini [10], Kistner [11], Nicolini [12], Creton [13], jusqu’à la dernière de Merchant et Pichot [14] qui ont étudié le registre global comportant 1 222 patients.
Sur toutes ces séries on retrouve les mêmes 3 complications thrombotiques postopératoires du début de l’inclusion.
De nombreuses séries rapportées dans la littérature ne révèlent pas d’ETVP [15-21].
Seules 3 séries rapportent un pourcentage plus important de complications thrombo-emboliques (Tableau I) :
- la première de Komenaka [22] rapporte 2 TVP sur 29 patients opérés mais, dans cette série, le cathéter était introduit par une incision inguinale et passé de haut en bas dans la grande veine saphène (GVS). Une de ces thromboses était une thrombose veineuse poplitée. Il est probable que cette procédure inhabituelle de haut en bas soit responsable de ce pourcentage plus élevé de TVP. Le nombre de patients revus n’est pas non plus précisé ;
- la deuxième série est celle de Hingorani [23] qui rapporte 12 TVP (16 %). La majeure partie des thromboses dépistées (11 sur 12) était des caillots flottants au niveau de la veine fémorale commune, une thrombose intéressait une veine gastrocnémienne. Chez 66 patients, 73 GVS avaient été traitées avec une procédure traditionnelle d’introduction par ponction percutanée du cathéter de bas en haut. Des phlébectomies complémentaires ainsi que des endoscopies sous-fasciales avaient été réalisées au cours de la procédure. A peu près 50 % des patients avaient été opérés sous anesthésie générale et l’autre moitié sous bloc fémoral. Dans cette série, l’âge moyen des patients était de 62 ans et la plupart (75 %) étaient classés 4 ou plus de la classification CEAP. Tous les patients avaient été réexaminés précocement par écho-Doppler.
Dans cette série, il n’y avait pas de différence significative concernant le risque d’ETVP suivant le sexe, le type d’anesthésie, la taille du cathéter utilisé 8 F versus 6 F et la réalisation simultanée de phlébectomies ou de section endoscopique de perforantes sous-fasciales. L’importance relative du nombre d’ETVP postopératoires dans cette série (16 %) par rapport à celles rapportées dans de nombreuses séries (1 %) ne peut s’expliquer que par l’importance de la classe CEAP des patients opérés dans cette série (75 % de classe 4) et la moyenne d‘âge des patients (62 ans). Il est en effet connu que le risque de thrombose profonde augmente avec l’âge ;
- la troisième est celle de Wagner [24] qui rapporte une ETVP non occlusive dans la veine fémorale sur 28 patients traités et revus en écho-Doppler précocement.
Une autre étude récente présentée à l’American Venous Forum en 2007 [25], non encore publiée, multicentrique, concernant l’étude du suivi du ClosureFASTTM ne met pas en évidence d’ETVP sur 252 traitements de GVS réalisés chez 194 patients. Le contrôle écho-Doppler postopératoire était aussi réalisé précocement après la procédure.
LASER
Malgré l‘imprécision de l’écho-Doppler postopératoire des séries concernant le laser, les complications dans les articles publiés jusqu’en septembre 2004 ont fait l’objet d’une revue systématique [26].
De nombreuses séries ayant bénéficié d’un écho-Doppler postopératoire systématique ne rapportent pas d’ETVP [27-34]. Cinq séries ont rapporté des TVP (Tableau II).
- Proebstle [35] sur 37 petites veines saphènes (PVS) traitées rapporte une ETVP poplitée. Dans cette série l’âge moyen des patients était de 60 ans et 73 % d’entre eux étaient classés 4 de la CEAP et 36 % classés 5 et 6.
- Anastasie [36] sur 311 patients traités (GVS et PVS) rapporte 2 TVP concernant les veines jumelles et soléaires. L’âge moyen des patients était de 45 ans et le nombre des patients revus n’est pas précisé.
- Timpermann [37] sur 111 patients traités rapporte une ETVP fémorale sous la forme d’un caillot flottant dans la JSF.
- Mozes [21] sur 39 patients traités et revus en écho-Doppler rapporte 3 cas d’ETVP dans la veine fémorale. Les patients étaient âgés respectivement de 51, 60 et 75 ans. Tous avaient été opérés sous anesthésie générale ou péridurale.
- Puggioni [38], sur 77 patients traités dont 70 % avaient eu un examen écho-Doppler postopéraoire, rapporte 3 ETVP dans la veine fémorale. Sur l’ensemble de ces patients la distance entre le thrombus de la JSF et la VFC était de 9,5 mm avec des extrêmes de – 20 mm (donc protrusion dans la VFC) à + 50 mm. La comparaison de cette donnée avec l’âge des patients a montré que cette distance était significativement plus petite chez les sujets âgés (P = .006).
Les séries plus récentes, du fait peut être de la plus large diffusion de cette technique, semblent rapporter un taux légèrement plus élevé de TVP.
DISCUSSION
Sans tenir compte du risque habituel de TVP post-opératoire de toute chirurgie des varices, le risque spécifique d’une ETVP venant de la JSF vers la VFC dépend de la maitrise technique de la procédure utilisée. En effet, les 3 TVP des premiers patients du Groupe Closure® ne se sont pas retrouvés sur le millier de patients inclus après.
Le passage d’un guide ou du cathéter dans la JSF et la veine fémorale avec des mouvements d’aller et venues peut être aussi un élément traumatisant.
Le cathéter le plus sécurisant est certainement le cathéter Closure Plus ® car il est très bien visible à l’écho-Doppler, son point de chauffage initial est extrêmement précis, et du fait de son mode de fonctionnement (c’est le passage du courant entre 2 points de contacts qui produit un échauffement entre ces 2 points de contacts), la procédure ne fonctionne pas si les électrodes sont au milieu de la veine fémorale.
Le cathéter ClosureFASTTM est moins bien visible et l’échauffement à son extrémité est certainement moins ponctuel. Dans notre expérience, avec le cathéter Closure Plus ® utilisé depuis 1998, nous n’avons jamais constaté de fermeture de la JSF à moins d’un centimètre de la valve terminale et aujourd’hui, avec le cathéter ClosureFASTTM utilisé depuis un an, nous avons déjà eu une fermeture complète faisant saillie dans la veine fémorale (Photo 4) . Il existe une façon de vérifier approximativement la position du cathéter Closure-FASTTM pendant l’injection de tumescence ; en effet, le thermocouple (qui mesure la température autour de l’élément chauffant) est situé à environ 6 cm de l’extrémité, l’injection per-opératoire de liquide de tumescence en regard du thermocouple lorsque le cathéter est en place se voit immédiatement par la baisse de température.
Concernant le laser, le repérage de son extrémité est aussi moins facile. Du fait d’une certaine inconnue concernant la diffusion thermique autour de l’extrémité de la fibre, il est préférable de se positionner légèrement en retrait de la valve terminale. Il est possible aussi que pendant les manipulations le traumatisme de la fibre laser sur la paroi soit plus important que celui du cathéter radiofréquence. De plus l’étendue de la thrombose après laser augmente avec l’âge des patients. La distance entre l’endothrombose et la veine fémorale diminue significativement chez les patients âgés [38].
En pratique courante, la rareté des TVP relevées après traitement endovasculaire peut s’expliquer aussi par le fait que les examens écho-Doppler ne sont pas tous réalisés systématiquement quelques jours après la procédure. Il est possible qu’un certain nombre de thromboses précoces se résorbent spontanément avant l’examen écho-Doppler réalisé plusieurs semaines après.
Bien que cela ne rende pas compte de la fréquence des complications de ces 2 techniques car leurs déclarations ne sont pas obligatoires, la FDA (Food and Drug Administration) par le rapport de données MAUDE (Manufacturer and User Facility Device Experience Database) nous donne un aperçu de l’ensemble des ETVP rapportées pour ces 2 techniques : 63 ETVP pour 112 complications déclarées après radiofréquence ClosurePlus® du 27/07/1999 au 16/08/2007 (http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfMAUDE/TextResults.cfm?dls=1&q=VNUS&pf=*&pn=10&sc=) et 6 ETVP pour 37 complications déclarées après LEV du 13/02/2003 au 16/08/2007 (http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfMAUDE/TextResults.cfm?dls=1&q=endovenous%20laser&pf=*&pn=10&sc=).
CONCLUSION
L’étude de ces séries montre que, mise à part des erreurs techniques qui peuvent par un mauvais positionnement induire un risque d’extension thrombotique veineuse profonde, ce risque augmente pour la petite veine saphène chez les sujets âgés, chez les patients classés 4, 5 ou 6 en classe CEAP. Pour ces patients il semble qu’une prescription systématique d’HBPM soit justifiée ainsi qu’un examen écho-Doppler précoce. Néanmoins, dans ces séries avec contrôles précoces écho-Doppler systématiques, le pourcentage reste assez faible, d’environ 1 % pour le laser. Concernant la radiofréquence utilisant le cathéter ClosurePlus®, le risque est presque nul. Concernant le cathéter ClosureFASTTM il faudra attendre la publication des premières études de suivi pour connaitre ce risque qui devrait être, lui aussi, faible, probablement plus voisin de celui du laser que de ClosurePlus®.
REFERENCES
- Perrin M. Traitement chirurgical endovasculaire des varices des membres inférieurs. Techniques et résultats. EMC (Elsevier Masson SAS, Paris) Techniques chirurgicales. Chirurgie vasculaire 2007 ; 43 : 161-C.
- Proebstle T.M., Sandhofer M., Kargl A., Gül D., Rother W., Knop J., Lehr H.A. Thermal damage of the inner vein wall during endovenous laser treatment : key role of energy absorption by intravascular blood. Dermatol Surg 2002 ; 28 : 596-600.
- Mordon S.R., Wassmer B., Zemmouri J. Mathematical modeling of endovenous laser treatment (ELT). Biomed Eng Online 2006 Apr. ; 25 (5) : 26.
- Weiss R.A. Comparison of endovenous radiofrequency versus 810 nm diode laser occlusion of large veins in an animal model. Dermatol Surg 2002 ; 28 : 56-61.
- Chandler J.G., Pichot O., Sessa C., Schuller-Petrovic S., Kabnick L.S., Bergan J.J. Treatment of primary insuffisance by endovenous saphenous vein obliteration. Vasc Surg 2000 ; 34 : 201-14.
- Chandler J.C., Pichot O., Sessa C., Schuler-Petrovic S., Osse F.J., Bergan J.J. Defining the role of extended sapheno-femoral junction ligation : a prospective comparative study. J Vasc Surg 2000 ; 32 : 941-53.
- Merchant R.F., Pichot O., Myers K.A. Four-year follow-up on endovascular radiofrequency obliteration of great saphenous reflux. Dermatol Surg 2005 ; 31 : 129-34.
- Merchant R.F., DePalma R.G., Kabnick L.S. Endovascular obliteration of saphenous reflux : a multicenter study. J Vasc Surg 2002 ; 35 : 1190-6.
- Merchant R. Jr, Kistner R.L., Kabnick L.S. Regarding « Is there an increased risk for DVT with the VNUS closure procedure ? » J Vasc Surg 2003 ; 38 : 628.
- Manfrini S., Gasbarro V., Danielsson G., Norgren L., Chandler J.G., Lennox A.F., Zarka Z.A., Nicolaides A.N. Endovenous management of saphenous vein reflux. Endovenous Reflux Management Study Group. J Vasc Surg 2000 ; 32 : 330-42.
- Kistner R.L. Endovascular obliteration of the greater saphenous vein : the Closure® procedure. Jpn J Phlebol 2002 ; 13 : 325-33.
- Nicolini P. Closure Group. Treatment of primary varicose veins by endovenous obliteration with the VNUS closure® system : results of a prospective multicentre study. Eur J Vasc Endovasc Surg 2005 ; 29 : 433-9.
- Creton D. et le groupe Closure. Oblitération tronculaire saphène par le procédé radiofréquence VNUS Closure® : résultats à 5 ans de l’étude multicentrique prospective. Phlébologie 2006 ; 59 : 67-72.
- Merchant R.F., Pichot O., Closure® Study Group. Long-term outcomes of endovenous radiofrequency obliteration of saphenous reflux as a treatment for superficial venous insufficiency. J Vasc Surg 2005 ; 42 : 502-9.
- Goldman M.P., Amiry S. Closure of the greater saphenous vein with endoluminal radiofrequency thermal heating of the vein wall in combination with ambulatory phlebectomy : 50 patients with more than 6-month follow-up. Dermatol Surg 2002 ; 28 : 29-31.
- Fassiadis N., Kianifard B., Holdstock J.M., Whiteley M.S. Ultrasound changes at the saphenofemoral junction and in the long saphenous vein during the first year after VNUS Closure®. Int Angiol 2002 ; 21 : 272-4.
- Rautio T.T., Perälä J.M., Wiik H.T., Juvonen T.S., Haukipuro K.A. Endovenous obliteration with radiofrequency-resistive heating for greater saphenous vein insufficiency : a feasibility study. J Vasc Interv Radiol 2002 ; 13 : 569-75.
- Weiss R.A., Weiss M.A. Controlled radiofrequency endovenous occlusion using a unique radiofrequency catheter under duplex guidance to eliminate saphenous varicose vein reflux: a 2-year follow-up. Dermatol Surg 2002; 28: 38-42.
- Sybrandy J.E., Wittens C.H. Initial experiences in endovenous treatment of saphenous vein reflux. J Vasc Surg 2002 ; 36 : 1207-12.
- Lurie F., Creton D., Eklof B., Kabnick L.S., Kistner R.L., Pichot O., Schuller-Petrovic S., Sessa C. Prospective randomized study of endovenous radiofrequency obliteration (Closure® procedure) versus ligation and stripping in a selected patient population (EVOLVeS Study). J Vasc Surg 2003 ; 38 : 207-14.
- Mozes G., Kalra M., Carmo M., Swenson L., Gloviczki P. Extension of saphenous thrombus into the femoral vein : a potential complication of new endovenous ablation techniques. J Vasc Surg 2005 ; 41 : 130-5.
- Komenaka I.K., Nguyen E.T. Is there an increased risk for DVT with the VNUS Closure® procedure ? J Vasc Surg 2002 ; 36 : 1311.
- Hingorani A.P., Ascher E., Markevich N., Schutzer R.W., Kallakuri S., Hou A., Nahata S., Yorkovich W., Jacob T. Deep venous thrombosis after radiofrequency ablation of greater saphenous vein : a word of caution. J Vasc Surg 2004 ; 40 : 500-4.
- Wagner W.H., Levin P.M., Cossman D.V., Lauterbach S.R., Cohen J.L., Farber A. Early experience with radiofrequency ablation of the greater saphenous vein. Ann Vasc Surg 2004 ; 18 : 42-7.
- Proebstle T.M., Vago B., Alm J., Göckeritz O., Wenzel C., Lebard C., Pichot O., Sessa C., Schmedt C.G., Noppeney T., Creton D. Treatment of incompetent great saphenous vein by radiofreqency segmental endovenous ablation (RSTA): first clinical experience. Communication présentée à l’American Venous Forum à San Diego en 2007. J Vasc Surg (submitted to publication).
- Mundy L., Merlin T.L., Fitridge R.A., Hiller J.E. Systematic review of endovenous laser treatment for varicose veins. Br J Surg 2005 ; 92 : 1189-94.
- Navarro L., Min R.J., Boné C. Endovenous laser : a new minimally invasive method of treatment for varicose veins – Preliminary observations using an 810 nm diode laser. Dermatol Surg 2001 ; 27 : 117-22.
- Min R.J., Zimmet S.E., Isaacs M.N., Forrestal M.D. Endovenous laser treatment of the incompetent greater saphenous vein. J Vasc Interv Radiol 2001 ; 12 : 1167-71.
- Gérard J.L., Desgranges P., Becquemin J.P., Desse H., Mellière D. Feasibility of ambulatory endovenous laser for the treatment of greater saphenous varicose veins : one-month outcome in a series of 20 outpatients. J Mal Vasc 2002 ; 27 : 222-5.
- Chang C.J., Chua J.J. Endovenous laser photocoagulation (EVLP) for varicose veins. Lasers Surg Med 2002 ; 31 : 257-62.
- Min R.J., Khilnani N., Zimmet S.E. Endovenous laser treatment of saphenous vein reflux : long-term results. J Vasc Interv Radiol 2003 ; 14 : 991-6.
- Proebstle T.M., Gül D., Lehr H.A., Kargl A., Knop J. Infrequent early recanalization of greater saphenous vein after endovenous laser treatment. J Vasc Surg 2003 ; 38 : 511-6.
- Oh C.K., Jung D.S., Jang H.S., Kwon K.S. Endovenous laser surgery of the incompetent greater saphenous vein with a 980-nm diode laser. Dermatol Surg 2003 ; 29 : 1135-40.
- Perkowski P., Ravi R., Gowda R.C., Olsen D., Ramaiah V., Rodriguez-Lopez J.A., Diethrich E.B. Endovenous laser ablation of the saphenous vein for treatment of venous insufficiency and varicose veins : early results from a large single-center experience. J Endovasc Ther 2004 ; 11 : 132-8.
- Proebstle T.M., Gül D., Kargl A., Knop J. Endovenous laser treatment of the lesser saphenous vein with a 940-nm diode laser : early results. Dermatol Surg 2003 ; 29 : 357-61.
- Anastasie B., Celerier A., Cohen-Solal G., Anido R., Boné C., Mordon S. et al. Laser endoveineux. Phlébologie 2003 ; 56 : 369-82.
- Timperman P.E., Sichlau M., Ryu R.K. Greater energy delivery improves treatment success of endovenous laser treatment of incompetent saphenous veins. J Vasc Interv Radiol 2004 ; 15 : 1061-3.
- Puggioni A., Kalra M., Carmo M., Mozes G., Gloviczki P. Endovenous laser therapy and radiofrequency ablation of the great saphenous vein : analysis of early efficacy and complications. J Vasc Surg 2005 ; 42 : 488-93.
Photo 1
Concernant le cathéter ClosurePlus® l’élévation thermique s’effectue sur la hauteur d’un disque circulaire de 3 mm de hauteur entre les 2 pôles + et – des électrodes appliquées sur la paroi veineuse

Photo 2
La zone de chauffage par contact et par radiation du cathéter ClosureFASTTM s’étend sur 7 cm le long de l’élément chauffant

Photo 3
Concernant le laser endoveineux, l’échauffement se produit au niveau d’une sphère lumineuse de chaleur située à l’extrémité de la fibre
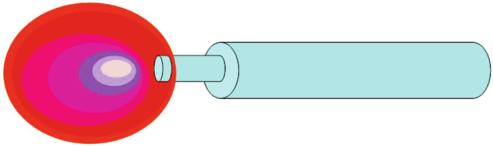
Photo 4
Extension thrombotique avec protrusion d’un thrombus de la jonction saphén- fémorale vers la veine fémorale (Photo : C Wunderlich)
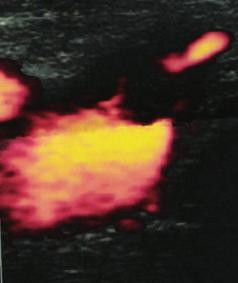
Tableau 1
Complications thrombo-emboliques : thrombose veineuse profonde (TVP) et embolie pulmonaire (EP) des études concernant ClosurePlus®
| Année | Membres | Membres revus | TVP | EP | |
| Chandler et le « Groupe Closure » [5-14] | 2000 | 301 | 223 | 3 | 1 |
| Goldman [15] | 2002 | 50 | 41 | 0 | 0 |
| Fassiadis [16] | 2002 | 127 | 99 | 0 | 0 |
| Rautio [17] | 2002 | 30 | 30 | 0 | 0 |
| Weiss [18] | 2002 | 140 | 140 | 0 | 0 |
| Sybrandy [19] | 2002 | 26 | 26 | 0 | 0 |
| Komenaka [22] | 2002 | 29 | ? | 2 | 0 |
| Lurie [20] | 2003 | 44 | 44 | 0 | 0 |
| Wagner [23] | 2004 | 28 | 28 | 1 | 0 |
| Hingorani [24] | 2004 | 73 | 73 | 12 | 0 |
| Mozes [21] | 2004 | 51 | 18 | 0 | 0 |
Tableau 2
Complications thrombo-emboliques : thrombose veineuse profonde (TVP) et embolie pulmonaire (EP) des études concernant le laser endoveineux
| Année | Membres | Membres revus | TVP | EP | |
| Navarro [27] | 2001 | 40 | 40 | 0 | 1 |
| Min [28] | 2001 | 90 | 90 | 0 | 0 |
| Gérard [29] | 2002 | 20 | 20 | 0 | 0 |
| Chang [30] | 2002 | 252 | 252 | 0 | 0 |
| Min [31] | 2003 | 504 | 499 | 0 | 0 |
| Proebstle [32] | 2003 | 109 | 104 | 0 | 0 |
| Proebstle [35] | 2003 | 37 | 37 | 1 | 0 |
| Anastasie [36] | 2003 | 311 | ? | 2 | 0 |
| Oh [33] | 2004 | 15 | 15 | 0 | 0 |
| Perkowski [34] | 2004 | 203 | 203 | 0 | 0 |
| Timpermann [37] | 2004 | 111 | 111 | 1 | 0 |
| Mozes [21] | 2004 | 56 | 39 | 3 | 0 |
| Puggioni [38] | 2005 | 77 | 54 | 3 | 0 |
| Date | 2007 |
| Auteurs | Phlébologie 2007 ;60 :359-66 D. CRETON Denis Creton, MD, EC A Paré, rue A Paré, 54100 F, Nancy, France - Telephone: 33 3 83 95 54 00; fax: 33 3 83 95 54 23; e-mail: [email protected]. |






